O primeiro estudo clínico em humanos de uma terapia gênica avançada para tratar atrofia muscular espinhal (AME) foi iniciado em Porto Alegre. O anúncio ocorreu na quinta-feira (26), em Brasília, durante atividade do Ministério da Saúde alusiva ao Dia Mundial das Doenças Raras, que é celebrado neste sábado (28).
Em parceria com o Ministério da Saúde, o Hospital de Clínicas de Porto Alegre (HCPA) e a Casa dos Raros, a Fiocruz conduz o projeto com a Gemma Biotherapeutics, Inc. (GEMMABio) — empresa americana detentora da tecnologia e patrocinadora do estudo no âmbito da Agência Nacional de Vigilância Sanitária (Anvisa).
O estudo clínico envolve o GB221, um produto de terapia gênica que integra a nova geração dessa classe de produtos, voltado ao tratamento da AME Tipo 1 (SMA1), considerada a forma mais grave da doença rara.
A AME se manifesta nos primeiros meses de vida. É causada por uma alteração no gene SMN1, responsável por produzir uma proteína essencial para o funcionamento dos neurônios responsáveis pelo comando dos movimentos. A ausência da proteína provoca a perda progressiva da força muscular, podendo comprometer a sobrevivência das crianças nos primeiros anos de vida.
O tratamento com GB221 é aplicado uma única vez com potencial de beneficiar o paciente por toda a vida, conforme divulgou a Casa dos Raros. Os impactos do tratamento também são de curto prazo, o que possibilitaria uma melhora na qualidade de vida do paciente em um curto espaço de tempo.
O primeiro paciente foi um bebê com diagnóstico de AME tipo 1, com menos de um ano de vida. O procedimento foi realizado em janeiro no Hospital de Clínicas de Porto Alegre (HCPA).
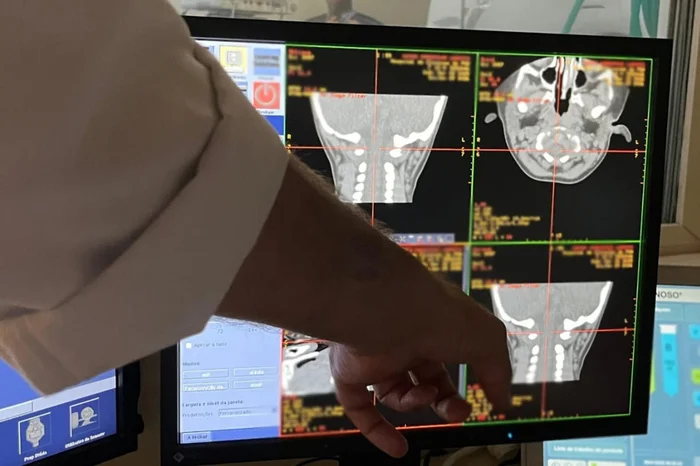
A terapia com o bebê foi aplicada via intracisterna magna (ICM), que leva o medicamento diretamente ao sistema nervoso central, permitindo que ele atinja mais regiões do cérebro e da medula espinhal. Conforme Roberto Giugliani, diretor executivo da Casa dos Raros e coordenador da pesquisa, o bebê foi avaliado e anestesiado antes do procedimento, que é guiado por imagem de tomografia.
— Quando a agulha chega ao ponto certo ali, se injeta o vírus que carrega o gene normal. E esse vírus, então, entra no sistema nervoso e começa lá a dar ordens para fabricar a proteína que mantém os neurônios funcionando — explica Giugliani.
Ele acrescenta que, nesta doença, os neurônios atrofiam pela falta da proteína que os protege. Então, é aplicada essa proteína deficiente no processo. Com o gene normal, a proteína que protege os neurônios passa a ser fabricada. Assim, o processo de regressão dos neurônios é interrompido.
— Administramos o gene que carrega a ordem para fabricar a proteína que falta ao bebê. É importante realizar esse procedimento cedo, porque quanto mais cedo tratar, mais neurônios são protegidos — adverte Giugliani. — Por isso, que é importante nessa doença fazer o teste do pezinho (que diagnostica precocemente doenças genéticas, metabólicas e infecciosas graves em recém-nascidos), para que se identifique logo.
Na primeira fase do estudo, o objetivo é avaliar a segurança e a tolerância do GB221. O protocolo prevê a inclusão gradativa de pacientes nesta fase. A previsão é que, nos próximos meses, o produto seja aplicado em uma segunda pessoa.
— O principal foco é identificar a segurança e a melhor dose do tratamento. Isso pode levar uns meses, talvez um ano. Depois, se parte para o estudo mais avançado, em que se utiliza a melhor dose que se selecionou, em um número um pouco maior de pacientes — frisa Giugliani.
Um produto desse porte costuma levar alguns anos para ser desenvolvido, como observa o coordenador do projeto. Porém, o plano para o GB221 é que o processo seja abreviado. Assim, estima-se que em dois ou três anos a terapia esteja aprovada para uso mais amplo.
Jonas Saute, professor do HCPA e integrante do projeto, aponta que os pacientes serão seguidos por 18 meses. Ele frisa que, como é a primeira vez que esse estudo está sendo realizado em seres humanos, é necessária a avaliação inicial desse primeiro caso:
— Há um comitê independente que avalia se é seguro ou não continuar. Se nos três primeiros pacientes isso se comprovar seguro, depois pode ser acelerada essa fase do recrutamento dos pacientes.
O professor acrescenta que haverá outros centros pelo Brasil. A expectativa é que a Unicamp e a USP também integrem o projeto.
Tratamento mais barato
Para Saute, o tratamento é um marco histórico. Ele observa que existem poucos estudos realizados no Brasil de terapias avançadas que envolvem algum tipo de modificação genética.
— Quando se tem um estudo de fase 1 e 2 (como é o caso com o GB221), significa que ou se está desenvolvendo a droga ou que a gente é visto como um desenvolvedor, de certa forma, em que a fase inicial acontece aqui. Já houve estudos de fase 1 e 2 desse tipo de terapia no Brasil, mas sempre com uma empresa do Exterior realizando e sem perspectiva depois de produção nacional — detalha Jonas.
O acordo de incorporação da tecnologia firmado entre o Instituto de Tecnologia em Imunobiológicos (Bio-Manguinhos/Fiocruz) e a GEMMABio prevê que os custos sejam significativamente menores que os valores atualmente praticados nos Estados Unidos em relação a terapias similares.
Giugliani ressalta que um tratamento desse porte pode custar em torno de R$ 7 milhões. Ao envolver diferentes instituições e parcerias, os valores são reduzidos no processo de testes. A transferência de tecnologia para que a Fiocruz fabrique a terapia no Brasil, sem custos de importação, também ajuda a diminuir o valor.
Em nota, o presidente da Fiocruz, Mario Moreira, destacou que “o acordo de incorporação de tecnologia também garante a abertura de caminhos para acesso a uma terapia gênica inovadora pela primeira vez no Sistema Único de Saúde“.
A Fiocruz domina a tecnologia de vetores virais, também usada para produção desta terapia gênica, desde a nacionalização da vacina Covid-19. “O desenvolvimento de vetores virais em condições de boas práticas de manufatura é um grande gargalo tecnológico em todo o mundo”, aponta nota da instituição. “O domínio da técnica confere ao Brasil um potencial inédito de protagonismo global nesta nova fronteira tecnológica”.
A diretora do Bio-Manguinhos/Fiocruz, Rosane Cuber, acrescentou que este acordo não apenas atende às demandas do SUS, mas fortalece o Complexo Econômico-Industrial da Saúde (Ceis), ao gerar autonomia tecnológica e economia para o país.
— Acho que se abre uma perspectiva muito interessante, muito favorável para o desenvolvimento de mais terapias desse porte — avalia Giugliani.
Há uma expectativa que seja inaugurada uma nova fase nas pesquisas sobre atrofia muscular espinhal, vislumbra Saute. O professor do HCPA acrescenta que existe previsão de haver outros tratamentos para outras doenças nesse mesmo modelo — e o pontapé inicial foi dado no Hospital de Clínicas de Porto Alegre.
Saute ressalta que as instituições brasileiras estão preparadas para realizar tratamentos de ponta em pacientes do SUS, transferindo rapidamente esses avanços para a população.
— Eu diria que o grande avanço é o modelo e a capacidade instalada. Talvez tenhamos o que há de mais avançado de terapia no contexto do SUS já sendo ofertado para os pacientes nessa primeira entrada, que é a oferta via pesquisa. Depois, quem sabe, isso virando um medicamento incorporado ao SUS, com as pessoas tendo acesso com um custo para o governo muito menor — conclui Jonas.
Source link
Você pode se precisar disso:
Produtos Recomendados

Ômega 3 1000mg Rico em EPA DHA com Selo IFOS e Vitamina E – 60 cápsulas Vhita-radardasaude
Ver na Amazon* Links de afiliado. Podemos receber uma comissão por compras qualificadas.
Conteúdo Indicado